Pozdrowienia mieszkańcy naszej strony!
Z roku na rok produkcja ropy naftowej staje się coraz bardziej złożona, a pozyskiwane z niej paliwo staje się coraz droższe. W krajach UE generalnie grożą, że przestaną produkować silniki benzynowe, chcą zastąpić wszystkie pojazdy samochodami elektrycznymi. Ale baterie litowe wciąż są dalekie od ideału, a przy okazji nie spieszą się, aby stać się idealnym. W najlepszym przypadku na jednym ładowaniu baterii litowej możliwe będzie pokonanie dystansu maksymalnie 700 km, po czym będziesz musiał ładować baterię przez około tydzień, a jeśli używasz zwykłego gniazdka do ładowania, zajmuje to zwykle dużo czasu. I wyobrażasz sobie, co się stanie, jeśli wszyscy zaczną stale ładować samochody elektryczne, jakie będą ogromne obciążenia w sieci elektrycznej i ile napięcia spadnie. Ogólnie rzecz biorąc, przyszłość akumulatorów litowych jest wciąż dość niejasna i co roku coraz więcej badań poświęcanych jest poszukiwaniu nowych opcji akumulatorów.
Jak wiadomo, najbardziej energochłonnym metalem jest aluminium. Już w naszych czasach na niektórych prototypach akumulatorów aluminiowych można przejechać około 2000 km bez ładowania, a ładowanie tego typu baterii zajmuje tylko 15 minut, po czym można przejść dalej na około 2000 km.
Ładowanie akumulatorów aluminiowych różni się od ładowania akumulatorów litowych. Niemniej jednak nie ma w tym nic skomplikowanego, wystarczy włożyć nowe aluminium, wylać elektrolit i wlać nowy elektrolit, wszystko jest zasadniczo takie samo jak benzyna samochód, tylko to jest samochód elektryczny i nie ma żadnych obciążeń w sieci energetycznej. Ponadto nie trzeba produkować ogromnej liczby gniazd z drutami o dużym przekroju, aby naładować wszystkie te samochody elektryczne.
Ale nie wszystko jest tu tak gładkie. Pozyskiwanie elektryczności z aluminium wcale nie jest tak łatwe, jak byśmy tego chcieli. Najpierw dowiedzmy się, na czym polega zasada aluminiowo-powietrznej baterii.
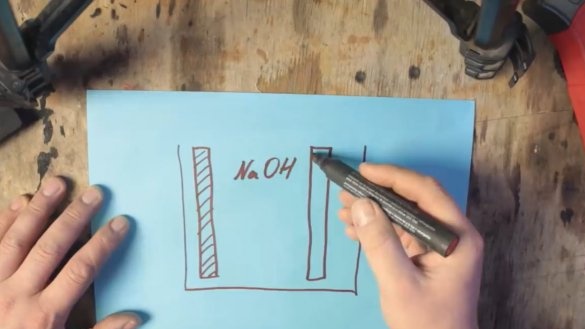
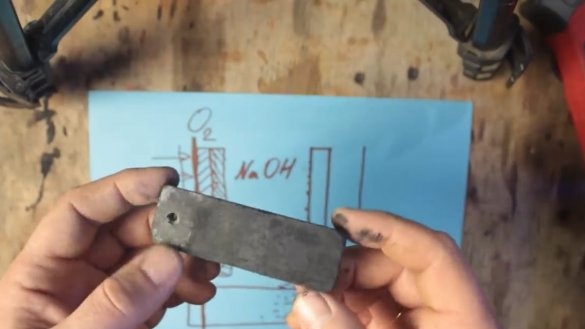
Aby taki akumulator zaczął działać, potrzebne będą 2 elektrody: jedna naturalnie z aluminium, a druga z grafitu. Obie elektrody znajdują się w roztworze elektrolitu.
Sól (NaCl) może być stosowana jako elektrolit, ale dzięki niej można podnieść napięcie do około 0,7 V. Napięcie elektrolitu alkalicznego (NaOH) można już zwiększyć, do około 1 V.
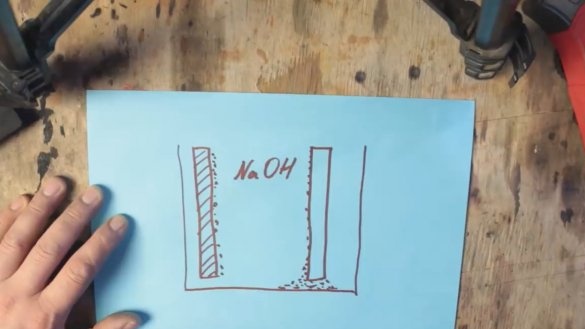
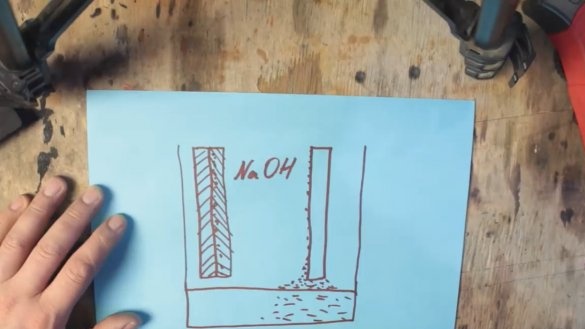
Podczas reakcji chemicznej aluminium powleka się warstwą wodorotlenku glinu (Al (OH) 3), który stopniowo tonie na dnie zbiornika. A na powierzchni elektrody grafitowej powstają pęcherzyki wodoru, co z kolei prowadzi do wzrostu rezystancji i spadku napięcia, proces ten nazywa się polaryzacją.
Pierwszy problem z wytrącaniem wodorotlenku glinu można wyeliminować przez zwykłe zwiększenie wydajności w miejscu, w którym zużyty produkt osiądzie, ale drugiemu problemowi można pomóc poprzez depolaryzującą masę na bazie tlenku manganu, która podczas działania zamieni się w wodorotlenek manganu.
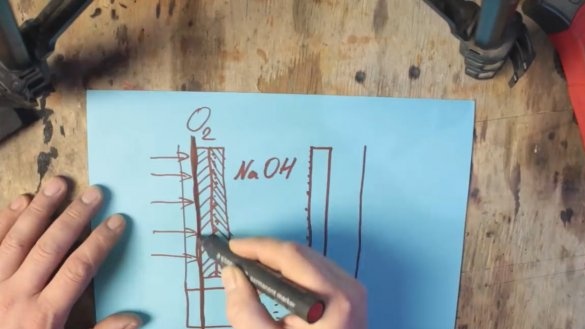
W rzeczywistości mamy zwykłą baterię alkaliczną, ale tylko bardzo dużą. Ale pojawia się nowy problem. Faktem jest, że tlenek manganu jest również zużywany i należy go również zmienić. I musimy zapewnić, że wydane zostanie tylko aluminium. Aby to zrobić, weź tlen z otaczającego powietrza. Tu zaczyna się aluminiowo-powietrzna bateria. Jedną ze ścian należy po prostu zastąpić przepuszczalną dla gazu membraną, a elektrodę grafitową należy zastąpić mieszaniną grafitu i tlenku manganu z nanocząstkami platyny lub srebra.
Tlenek manganu z nanocząstkami metali szlachetnych nie reaguje, ale działa jak katalizator, dzięki czemu wodór z elektrolitu jest utleniany przez tlen w powietrzu.
Technologia wytwarzania tlenku manganu z wtrąceniami nanocząstek srebra w zasadzie nie jest skomplikowana i można ją wypróbować w warunkach rzemieślniczych. Ale w tym artykule omówimy, jak zrobić najbardziej budżetową opcję dla baterii, która otrzymuje energię z aluminium. Poniższe instrukcje pochodzą z kanału YouTube Fiery TV. Więcej informacji w oryginalnym wideo autora:
Maksymalnie budżetowa wersja grafitu to letnie wkładki stykowe do trolejbusów. Można je znaleźć całkowicie za darmo na końcowych przystankach trolejbusu lub można je kupić, nie są drogie, autor znalazł je w sprzedaży po 22 rubli za sztukę.
Następnie potrzebujemy zasady. Oto narzędzie do czyszczenia rur w swoim składzie zawiera stuprocentowe zasady alkaliczne sodu.
Aby rozpocząć reakcję alkaliczną, potrzebujemy tylko trochę, wystarczy 1 g zasady na 0,5 l wody.
Przede wszystkim sprawdźmy, czy w tej baterii naprawdę potrzebna jest elektroda grafitowa. Dla doświadczenia weźmy tę elektrodę ze stali nierdzewnej.
Teraz wkładamy aluminiową płytkę i elektrodę ze stali nierdzewnej do alkaliów, podłączamy multimetr i widzimy, ile woltów się pojawi.
Jak widać, okazało się, że około 1,4 V. Teraz sprawdźmy prąd zwarciowy.
Prąd zwarciowy okazał się w okolicach 20mA. Jakie wnioski można wyciągnąć: teoretycznie w ekstremalnych warunkach można zamontować baterię kubków ze stali nierdzewnej i folii aluminiowej.
Następnie będziemy mieli elektrodę miedzianą wykonaną z miedzi elektrycznej.
Jak możemy zaobserwować, napięcie okazało się nieco wyższe niż 1,4 V, ale prąd zwarciowy był początkowo wysoki, ale potem zaczął dość szybko opadać, a miedź również zaczęła pokrywać się ciemną powłoką, najprawdopodobniej efekt ten został spowodowany przez zanieczyszczenia w wodzie, ponieważ W tym eksperymencie autor wziął kran z kranu.
Teraz zanurz elektrodę grafitową w roztworze elektrolitu.
Za pomocą tej elektrody uzyskano napięcie 1,3 V. Prąd zwarciowy zatrzymano w okolicach 17 mA. Na pierwszy rzut oka wydaje się, że elektroda ze stali nierdzewnej jest bardziej wydajna, ale powierzchnia elektrody ze stali nierdzewnej jest większa, więc nie wiadomo jeszcze, który grafit lub stal nierdzewna jest lepsza.
Ponieważ grafit ma dość duży opór, musisz jakoś sobie z tym poradzić. Konieczne jest wykonanie elektrod z materiału dobrze przewodzącego, a grafit powinien znajdować się tylko na jego powierzchni.Zdecydowano się wiercić grafit, a w powstałych otworach wyciąć gwint dla śrub M6.
Rezultatem jest stalowa elektroda z powłoką grafitową.
Rezystancja grafitu niewierconego wynosi około 4,5 oma, ale grafitu wierconego wynosi około 1,7 oma.
Na twarzy wzrośnie spadek oporu, a w konsekwencji skuteczność struktury. W dalszych eksperymentach użyjemy wody destylowanej.
Pierwszy eksperyment z elektrolitem, w którym 4 g alkaliów na 1 litr wody.
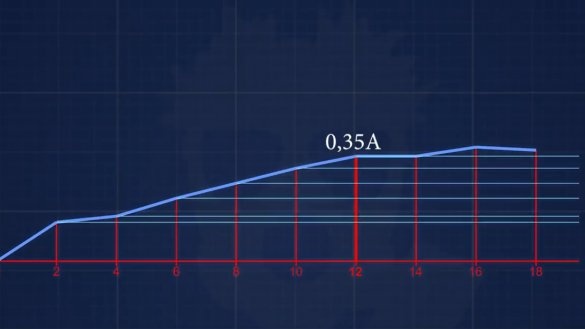
Prąd zwarciowy okazał się 150mA. Następny elektrolit ma stężenie 6 g alkaliów na 1 litr. I tak dalej, za każdym razem zwiększamy stężenie o 2 g, aż osiągniemy stężenie, przy którym prąd nie wzrośnie.
Chociaż taka prosta bateria nie ma dużej wydajności prądowej, ale taka bateria może działać bardzo długo, a każde aluminium można wykorzystać jako elektrody, które można łatwo stopić w elektrody o dowolnym kształcie, na przykład puszki aluminiowe różne napoje alkoholowe i bezalkoholowe, folia czekoladowa itp.
W rezultacie po wszystkich eksperymentach z różnymi stężeniami elektrolitu staje się jasne, że przy takiej konstrukcji akumulatora nie ma sensu dodawać więcej niż 12 g alkaliów do 1 litra wody, to znaczy, że otrzymujemy około 1% roztwór.
Następnie autor zmontował kolejny klip, składający się z 3 elektrod.
Dwie baterie dają wyższe napięcie i mniej strat, więc wynik jest lepszy.
A teraz weźmy wiadro elektrolitu, duży kawałek aluminium i 2 elektrody ze stali nierdzewnej.
W wiadrze stężenie elektrolitu 10 g / 1 l. Prąd szczytowy 1,3A, spadł do 520mA. Przy całej tej ogromnej powierzchni stali nierdzewnej nie dorównywał grafitowi, ponieważ okazało się, że z grafitem wynosi 600mA. Nawiasem mówiąc, podczas reakcji uwalnia się wodór, który można również zbierać i wykorzystywać jako źródło energii. Krótko mówiąc, jest miejsce na rozwój. To wszystko na teraz. Dziękuję za uwagę. Do zobaczenia wkrótce!